Диагностика АФС
В настоящее время существует несколько подходов к алгоритму диагностики АФС и ВА в частности: ISTH (международное общество по тромбозам и гемостазу), BSH (Великобритания) и CLSI (США). Для включения в данный раздел были выбраны, как наиболее авторитетные и распространенные, рекомендации ISTH, а также данные производителя реагентов – компании Stago.
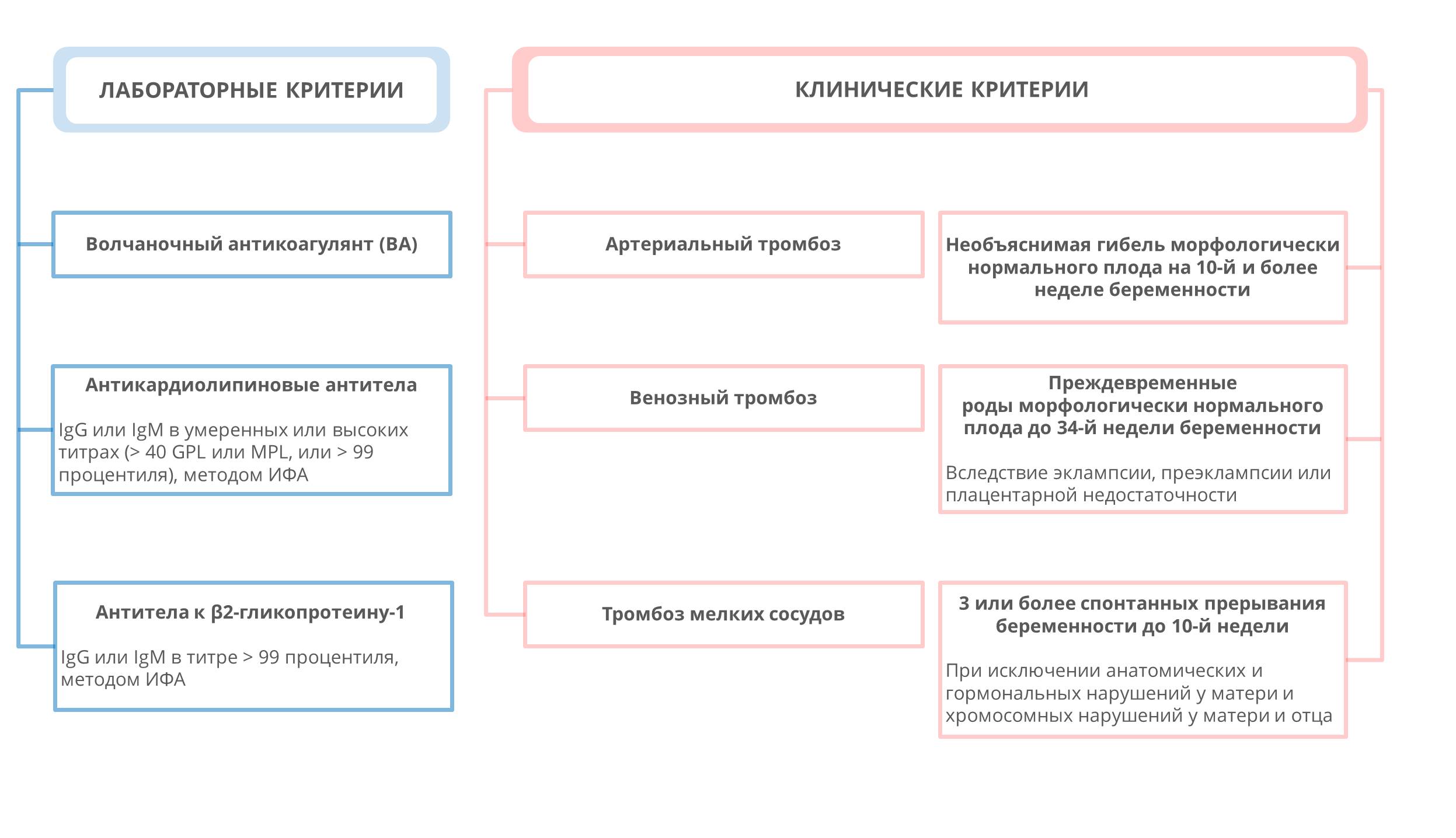
Диагностика АФС основана на клинических и лабораторных критериях. Для постановки диагноза АФС необходимо присутствие как минимум одного клинического и одного лабораторного критерия.
К лабораторным критериям диагностики АФС относятся определение антител к кардиолипину (аКЛ), антител к β2-GPI и волчаночного антикоагулянта. Несмотря на рекомендацию определять антитела классов IgG и IgМ (но не IgA и не суммарные), значение определения антител класса IgM не до конца определено в связи со слабой корреляцией уровня данных антител с клиническими симптомами. Кроме того, при интерпретации результатов исследования антител класса IgM необходимо учитывать возможное присутствие криоглобулинов и ревматоидного фактора.
Выявление антител к β2-GPI особенно важно у пациентов с подозрением на АФС и с отрицательным результатом тестов на присутствие волчаночного антикоагулянта. В диагностике АФС определение антител к β2-GPI является более специфичным, чем определение антител к кардиолипину. В 3-10% случаев присутствие антител к β2-GPI у пациентов с AФС может быть единственным положительным лабораторным критерием. Несмотря на отсутствие стандартизации, методика определения антител к β2-GPI обладает более высокой воспроизводимостью по сравнению с методикой определения антител к кардиолипину.
Далее мы рассмотрим методику выполнения определения волчаночного антикоагулянта.
Выбор пациентов: определение волчаночного антикоагулянта должно проводиться только у пациентов с высоким риском АФС. Необходимость назначения исследования для выявления ВА определяют на основании клинических характеристик пациента:
Высокая:
- неспровоцированный эпизод венозного или артериального тромбоза у лиц <50 лет
- тромбоз нетипичной локализации
- потеря беременности на поздних сроках
- тромбоз или патология беременности у лиц с аутоиммунными заболеваниями (СКВ, ревматоидный артрит, аутоиммунная тромбоцитопения, аутоиммунная гемолитическая анемия).
Средняя:
- случайное выявление удлинения АЧТВ у асимптоматических пациентов
- привычное невынашивание беременности на ранних сроках
- спровоцированный ВТЭ у молодых пациентов.
Низкая:
- венозный или артериальный тромбоз у пожилых пациентов
Общие положения:
- Лабораторные исследования по выявлению ВА рекомендуется выполнять в отсутствии антикоагулянтной терапии (через 1-2 недели после окончания приема АВК или при МНО <1.5. В случае использования НМГ – через >12 часов после введения препарата). Некоторые реагенты с ядом гадюки Рассела (dRVV) содержат ингибитор гепарина и позволяют проводить исследования для образцов плазмы с концентрацией НФГ до 0.8 МЕ/мл.
- При МНО в диапазоне 1.5 - 3.0 допускается проводить исследования с выполнением предварительного разведения образца пулированной нормальной плазмой в отношении 1:1. Полученные результаты следует интерпретировать с особой осторожностью.
- Результаты исследований, полученные у пациентов в острой фазе тромботического события необходимо интерпретировать с осторожностью в связи с возможностью получения пациентом НФГ, а также в связи с реактивным повышением активности ф.VIII.
- К финальному результату исследования, выдаваемому лабораторией, обязательно должен прилагаться комментарий, поясняющий является ли результат положительным / отрицательным на наличие ВА.
- Если лаборатория не выполняет полный перечень рекомендуемых исследований для выявления ВА - результате теста необходимо указать, какая методика была использована и рекомендации по проведению дополнительных исследований.
- В случае подозрения на присутствие в образце антикоагулянтов (варфарин, гепарины, ПОАК) к результату теста прилагается соответствующий комментарий.
- ВА считается “положительным” при получении положительного результата в подтверждающем тесте хотя бы одной методики определения ВА. См. следующий пункт.
- В случае получения положительного результата определения ВА, необходимо в обязательном порядке провести повторное тестирование для данного пациента через, как минимум, 12 недель.
- В случае получения повторного положительного результата через >12 недель – присутствие ВА считается подтвержденным.
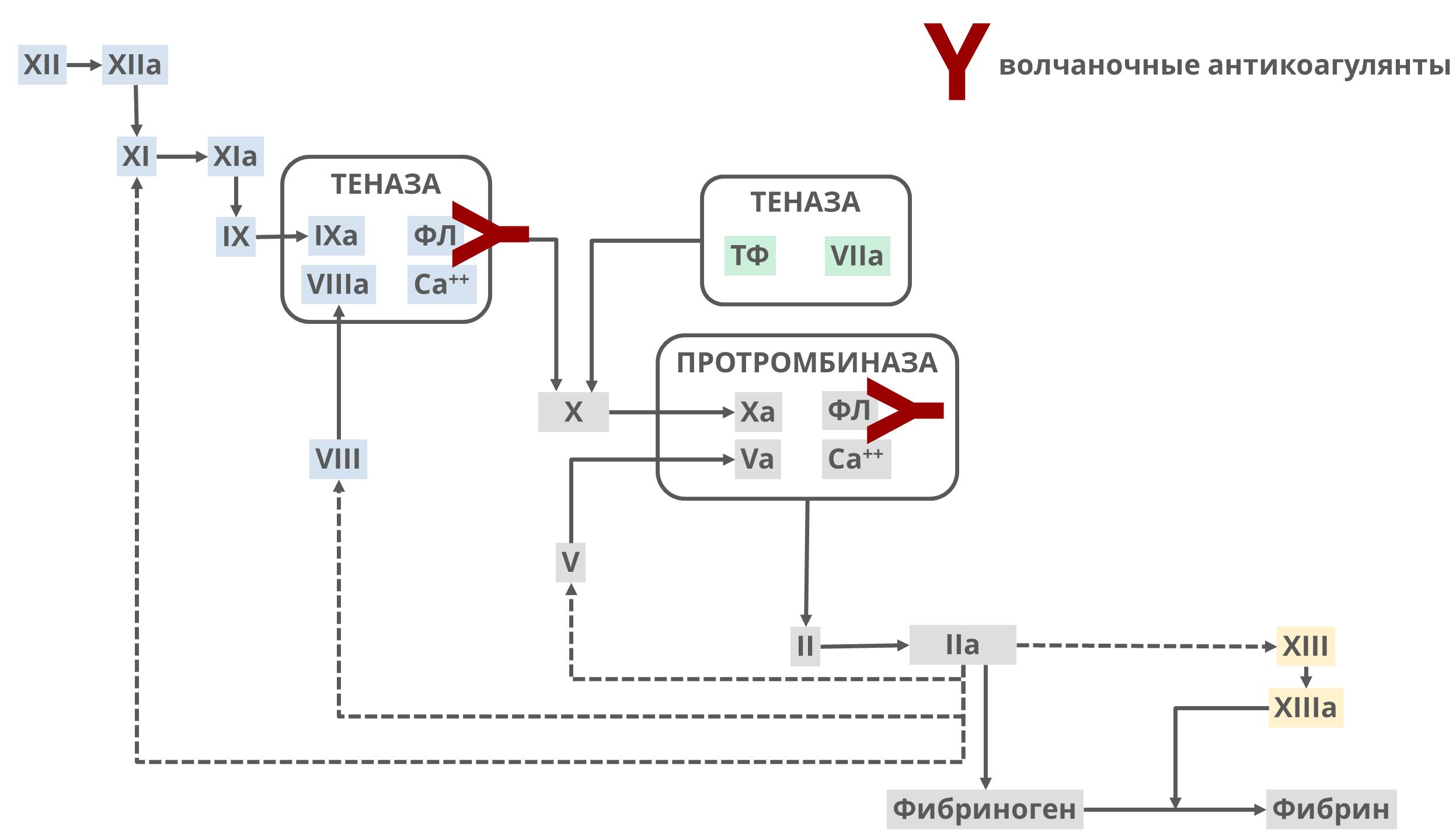
Для диагностики ВА применяются клоттинговые тесты. Их использование основано на способности ВА удлинять время свертывания в фосфолипид-зависимых тестах за счет конкурентного связывания с фосфолипидами в реакционной смеси.
Соблюдение условий преаналитического этапа исследований для выявления волчаночного антикоагулянта является одним из ключевых факторов в диагностике АФС:
- Используется только свободная от тромбоцитов плазма. Присутствие остаточного количества тромбоцитов в исследуемой плазме может оказать влияние на результаты фосфолипид-зависимых клоттинговых тестов посредством нейтрализации антифосфолипидных антител (присутствующих в образце плазмы) тромбоцитарными фосфолипидами с получением ложноотрицательных результатов исследований.
- Для получения свободной от тромбоцитов плазмы необходимо выполнить центрифугирование цельной крови при 2000g в течение 15 минут, затем перенести надосадочный слой плазмы в пластиковую пробирку и провести ее центрифугирование при >2500g в течение 10 минут.
- В случае необходимости отложенного выполнения исследований, полученная путем двойного центрифугирования плазма может быть заморожена при -70°С (при хранении <1 месяца возможна заморозка при -20°С). Осуществлять заморозку плазмы рекомендуется сразу после центрифугирования.
- Разморозку плазмы необходимо выполнять при 37°С (водяная баня, термостат) для исключения образования криопреципитатов.
Выбор методик тестирования
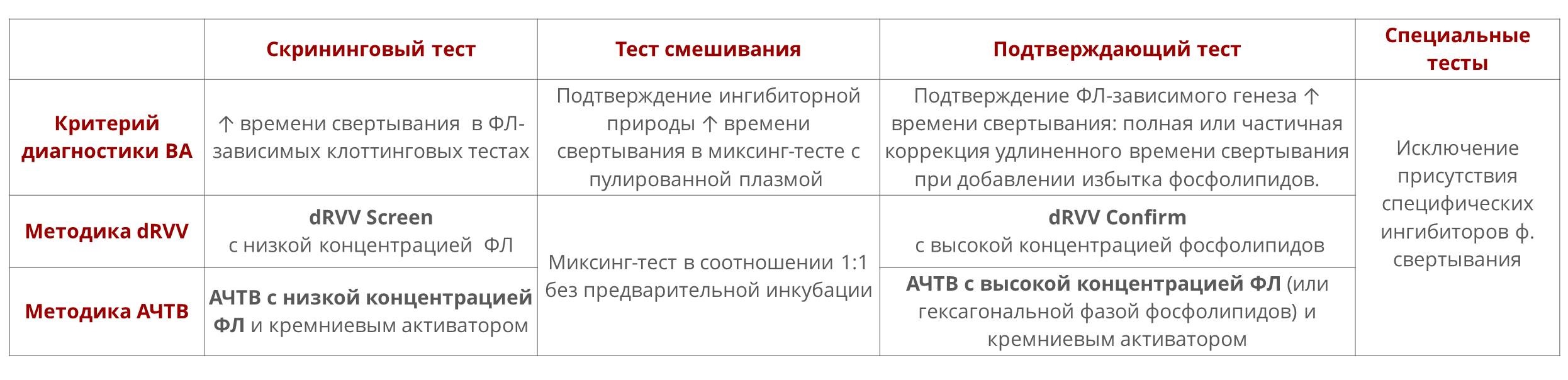
В настоящее время не существует единого теста, чувствительного ко всем ВА. В данной связи рекомендуется использовать 2 типа тестов, основанных на разных принципах метода:
- Методика с ядом гадюки Рассела (dRVV, diluted Russel Viper Venom) рекомендована как тест “первой линии”.
- Методика чувствительного к ВА АЧТВ с кремниевым активатором и малым количеством фосфолипидов. Использование каолина и эллаговой кислоты в качестве активаторов не рекомендуется в связи с ограничениями методов детекции и низкой чувствительностью к ВА.
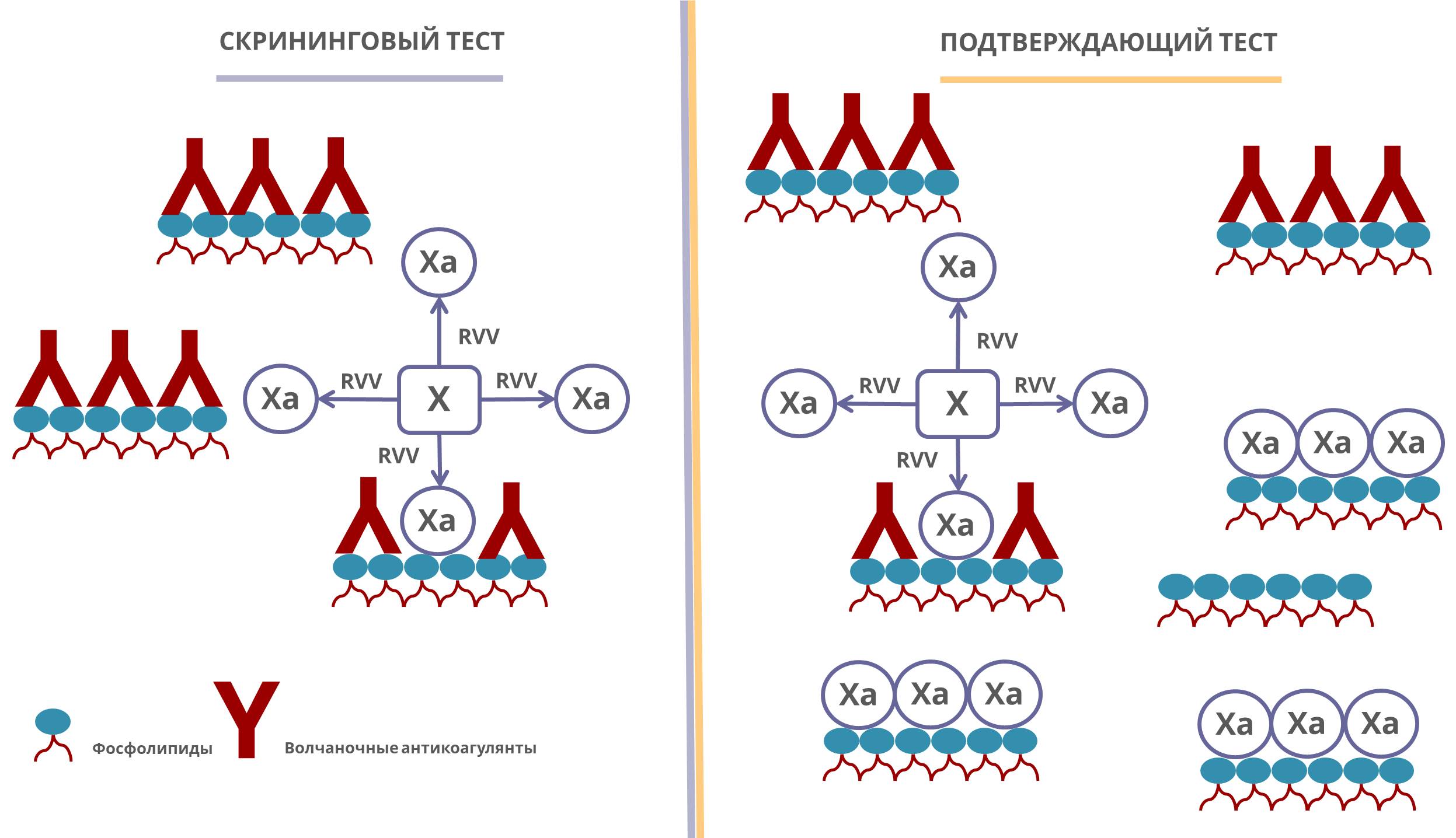
Принцип тестов для определения ВА с использованием скринингового и подтверждающего тестов основан на первичном использовании реагента с малым количеством фосфолипидов (скрининговый реагент) для измерения удлинения времени свертывания по сравнению с референсным ВС. Причина удлинения времени свертывания в скрининговом тесте – конкурентное действие ВА по связыванию с ФЛ реакционной смеси, в результате чего количества ФЛ не хватает для осуществления коагуляции в пределах референсного ВС. Последующее использование реагента с избытком ФЛ (подтверждающий реагент) обеспечивает связывания ВА с ФЛ и доступность остаточного количества ФЛ для более быстрого формирования сгустка, чем в скрининговом тесте. Данные процессы схематично представлены на рисунке ниже:
Тесты, использование которых не рекомендовано: протромбиновое время с разведением (вариабельность тромбопластинов), методики с экарином и текстарином (отсутствие стандартизации), каолиновое время свертывания (низкая воспроизводимость).
Тест смешивания (mixing test, миксинг тест)
Тест смешивания выполняется с использованием исследуемой и пулированной нормальной плазмы в соотношении 1:1 без предварительной инкубации. Данный тест выполняется с целью дифференцировки присутствия дефицита активности факторов свертывания (как истинного, так и вследствие приема антикоагулянтов) от присутствия специфических и неспецифических (ВА) ингибиторов.
Источники пулированной плазмы:
- Home-made пулированная нормальная плазма, подготовленная по обычному алгоритму и активность всех факторов свертывания в которой близка к 100%. Выполнение двойного центрифугирования необходимо для получения плазмы, содержащей менее 10 000 тромбоцитов/мкл. Хранение при -70°С.
- Коммерческая пулированная нормальная плазма, отвечающая требуемым характеристикам.
Интерпретация теста смешивания выполняется с использованием индекса Рознера (RI) по формуле: RI = [(b - c) / a] х 100 где a, b, c являются значениями времени свертывания плазмы пациента, смеси и нормальной плазмы соответственно. Время свертывания считается скорректированным, если RI меньше 12%. RI больше 15% означает отсутствие коррекции. Значения 12 - 15% являются «серой зоной».
- если в смеси наблюдается коррекция - ингибитор отсутствует, наблюдается дефицит фактора/ов свертывания
- если в смеси наблюдается отсутствие коррекции - в плазме присутствует ингибитор.
Исключение специфических ингибиторов факторов свертывания
Выявление специфических ингибиторов к конкретным факторам свертывания (в первую очередь к ф.VIII или ф.IX) имеет важное значение в дифференциальной диагностике ВА и дальнейшем ведении пациентов. Данный тип исследований включает определение активности факторов свертывания, и, при необходимости, выполнение более специализированных тестов для выявления количества ингибитора.